为简化临床试验资料递交流程,经我院机构办与伦理委员会讨论,现将临床试验过程中文件递交流程更新如下:
1、线上审批
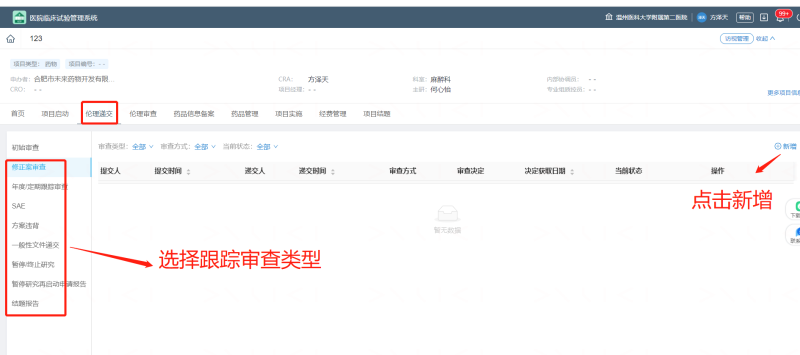
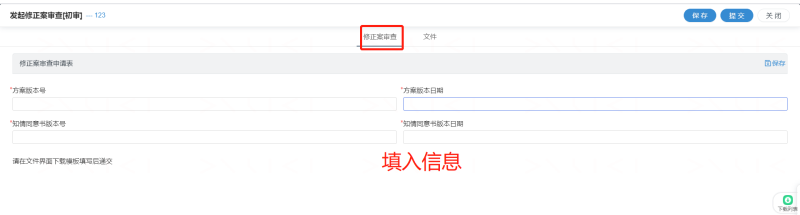
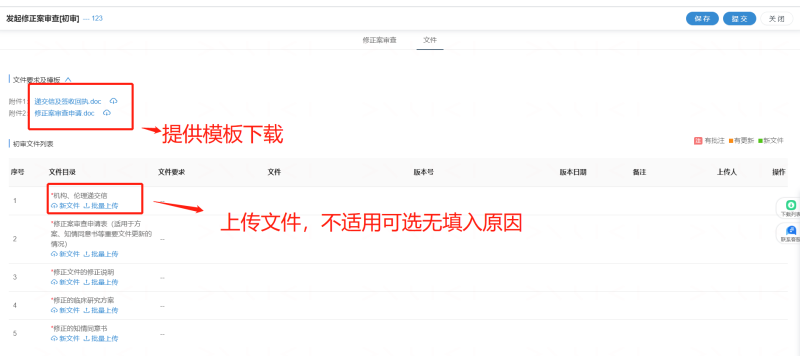
1)CRA登录太美 eSite 临床试验项目管理系统(网址:https://wzhealthgcp.trialos.com/login/ ),进入项目后,选择跟踪审查的类型,按系统提示上传文件,具体如下图:
*所有资料线上审批时可以不需要签字盖章
2)流转至PI处,PI审核后,流转至机构办质控员处;
*若系统中未检索到PI,请按《PI、CRA及CRC账号开通及变更流程》申请开通账号。
3)机构办质控员审批通过后,流转至伦理秘书;
2、递交纸质
(1)机构办质控员预审批完成,CRA需在2个工作日内递交纸质资料至机构办公室及伦理委员会,伦理秘书待接收到纸质材料时,再在系统上点击受理,安排后续审查形式。
(2)递交纸质递交信一式3份,完整附件资料2份,要求:1)资料与线上预审批一致;2)签字盖章完整,PI签字日期应与PI审核系统时间一致。
(3)纸质资料要求先递交机构办,再递交伦理委员会。机构办保留1份递交信;伦理委员会保存1份递交信+1份完整附件资料;剩余1份递交信+1份完整附件资料保存至科室研究者文件夹,待归档时统一归档至机构档案室。
3、注意
1)临床试验过程中文件递交相关模板请于《表格模板汇总》或“医院官网-科研教学-医学伦理-《GCP机构办立项的研究项目伦理审查申请》”下载
2)本流程从2022年3月29日正式开始实施。